Поисковый фильтр
Период публикации
от
до
Раздел страницы
Подпаздел страницы
catalogul tematic
Каталог авторов
Catalogul revistelor
Каталог учреждений
Ключевое слово
Искать через google
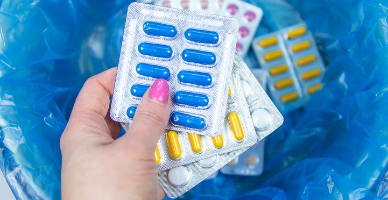
Obiectivul de bază al Regulamentului constă în implementarea sistemului național de colectare a medicamentelor expirate de la populație până la 31 decembrie 2025.

Modul de colectare, stocare temporară de către întreprinderile și instituțiile farmaceutice a medicamentelor expirate, precum și transmiterea acestora către operatorii autorizați pentru gestionarea deșeurilor farmaceutice, va fi reglementat în temeiul Regulamentului privind gestionarea deșeurilor farmaceutice, proiectul căruia a fost inclus pe ordinea de zi a ședinței secretarilor generali de stat din 7 iulie curent.

Importul materiei prime medicamentoase, a materialelor, articolelor, ambalajului primar şi secundar utilizate la producerea medicamentelor de uz uman și prepararea formelor medicamentoase magistrale ar putea fi permis doar prin autorizația de import, eliberată de către Agenția Medicamentului și Dispozitivelor Medicale.

Personalul farmaceutic este compus din farmacişti-specialişti cu studii farmaceutice superioare şi laboranţi-farmacişti specialişti cu studii farmaceutice medii. În tabelul de mai jos găsiţi norme juridice în vigoare cu privire la garanţii acordate personalului farmaceutic. Cetăţenii străini şi

Acordarea scutirilor de TVA fără drept de deducere aferente importului de materii prime, materiale și ambalaje de către producătorii autohtoni de medicamente va avea loc în baza autorizației de import eliberate de către Agenția Medicamentelor și Dispozitivelor Medicale, fără aplicarea unei liste suplimentare aprobate la nivel de hotărâre de Guvern. Potrivit proiectului de lege pentru modificarea unor acte normative, modificările propuse în Codul fiscal, Legea nr.1380/1997 cu privire la tariful vamal și Legea nr.1456/1993 cu privire la activitatea farmaceutică au drept scop eliminarea impedimentelor la importul mărfurilor enumerate supra, ceea ce va simplifica și va facilita importul acestora.

В парламенте зарегистрирована инициатива о внесении изменений и дополнений в Закон о фармацевтической деятельности, Закон о лекарственных средствах ветеринарного назначения и Кодекс о правонарушениях. Поправки направлены на обеспечение сбора у населения медицинских отходов, а именно просроченных или испорченных лекарств. Авторы проекта предлагают, чтобы фармацевтические предприятия и учреждения обеспечивали сбор у населения лекарств, фармпрепаратов и парафармацевтических препаратов с истекшим сроком годности, а также испорченных/поврежденных.

În anul 2020 în Republica Moldova erau înregistrați 2928 titulari de licență, iar din numărul total de licențe valabile 72% au fost eliberate pentru șapte genuri de activitate: cu metale preţioase – pentru 455 entități; de utilizare a canalelor sau frecvenţelor radio şi/sau serviciilor de comunicaţii electronice – 417; pentru activitate farmaceutică – 356; pentru unităţile de schimb valutar – 304. Totodată, 229 acte permisive au fost valabile pentru activitatea asociațiilor de economii și împrumut, 202 – pentru importul și comercializarea cu amănuntul a carburanților, iar 137 – pentru producţia alcoolică autohtonă.

Agenţia Medicamentului şi Dispozitivelor Medicale (AMDM) a înregistrat prețurile de producător pentru 229 de medicamente. În monedă națională prețurile sunt în medie cu 4,7% mai mici comparativ cu aceeaşi perioadă a anului trecut.

Agenţia Medicamentului şi Dispozitivelor Medicale (AMDM) a înregistrat 358 de preparate farmaceutice cu preţuri de producător noi, în luna octombrie 2017.

Atribuțiile Agenției Medicamentului și Dispozitivelor Medicale (AMDM) de coordonare a procesului de aprovizionare cu medicamente a spitalelor vor fi preluate de Centrul pentru achiziții publice centralizate în sănătate. În Monitorul Oficial a fost publicată Hotărârea Guvernului care prevede crearea acestui Centru.

Măsurile urgente întreprinse de Agenția Medicamentului și Dispozitivelor Medicale (AMDM) pentru redresarea situației pe piața farmaceutică din Moldova dau rezultate vizibile chiar din primele zile, se scrie în cadrul unui comunicat al instituției.

Agenția Medicamentului și Dispozitivelor Medicale a inițiat procedura de control în întreprinderile farmaceutice. Controalele sunt efectuat ca urmare a solicitării Guvernului de a soluționa unele probleme identificate în domeniul medicamentului și a activității farmaceutice.

Agenția Medicamentului și Dispozitivelor Medicale promite ca în câteva săptămâni va veni cu soluții pentru lipsa unor tipuri de medicamente pe piața farmaceutică din Moldova.

Dacă până la începutul lunii octombrie, în Republica Moldova activau 27 de producători de medicamente, după implementarea noilor reguli GMP, numărul acestora s-a redus la 13, anunţă Agenţia Medicamentului și Dispozitivelor Medicale (AMDM). Se întâmplă după ce la 1 octombrie curent, în urma unui ordin al ministerului Sănătăţii, implementarea Regulilor de Bună Practică de Fabricație a medicamentelor (GMP) a devenit obligatorie.
Счет пользователя создан успешно. Для подтверждения регистрации пройдите по подтверждающей ссылке, действительной в течение 30 календарных дней, отправленной на указанный в формуляре регистрации е-майл.
Задайте нам вопрос
Есть необходимость получить ответ на вопрос, или хочешь предложить тему для статьи, поясняющей практические аспекты деятельности? Зарегистрируйся, отправь вопрос или тему для статьи и в кратчайшие сроки получишь ответ эксперта на электронный адрес или в профиле на странице.
Е-майл *
Заказать услугу по телефону
Введите правильные данные и вскоре с вами свяжется оператор
Имя *
Фамилия *
Е-майл *
Телефон *
Отзыв
Для отслеживания статуса обработки отправленного отзыва, рекомендуем зарегистрироваться на странице. Таким образом ответ, отправленный Вам периодическим изданием «Monitorul Fiscal FISC.md» сохранится и отразится в Вашем профиле. В случае отправки отзыва без регистрации, ответ будет отправлен на ваш е-майл.
Е-майл *
Е-майл *
Уважаемый пользователь
Мы настоятельно рекомендуем вам оформить бесплатную подписку на Newsline.
